自新冠疫情暴发以来,新冠病毒(SARS-CoV-2)、流感病毒与呼吸道合胞病毒(RSV)的交替或叠加流行,给全球医疗系统带来巨大压力。联合疫苗通过一次接种即可实现多重疾病防护,具有减少注射次数、提高接种依从性、扩大免疫覆盖率、成本效益优良等多重优势,已成为世界卫生组织(WHO)、全球疫苗免疫联盟(Gavi)等机构重点倡导的研发方向。基于mRNA疫苗技术研发可抵御多种呼吸道病原体的高效联合疫苗,是具备可行性的重要攻关方向,而抗原间免疫干扰、免疫持久性仍是当前面临的关键挑战。
针对上述挑战,我院夏宁邵教授、李少伟教授团队依托mRNA技术平台,设计并构建了一款针对三种呼吸道病毒、包含8种抗原组分的SIR联合疫苗,涵盖新冠病毒3种变异株的受体结合域(RBD),流感病毒的4种代表性亚型(H1N1、H3N2、B/Victoria、B/Yamagata)的血凝素头部区(HAhr),以及RSV的融合前F蛋白(pre-F),在抗原广谱性和免疫增强方面形成了独特优势。为进一步增强免疫反应,团队在SIR联合疫苗基础上引入了TLR-9激动剂CpG-ODN 1018,最终获得优化版SIRC疫苗。CpG-ODN 1018的加入显著延长了抗原在注射部位的表达时间,增强Th1型免疫应答,在不破坏各抗原免疫平衡的前提下,实现了对三种病毒抗原的免疫增强。
研究显示,SIRC疫苗在小鼠模型中可高效诱导针对三种病毒的体液免疫与细胞免疫应答。其诱导产生的结合抗体、中和抗体滴度与单价疫苗相当或者更高;在细胞免疫方面,SIRC疫苗诱导的针对三种的病毒的IFN-γ⁺ T细胞应答,较SIR疫苗最高提升约4.5倍,较单价疫苗最高提升约10倍,并成功诱导CD4⁺和CD8⁺效应记忆T细胞(TEM)形成,为长期免疫保护奠定基础。安全性评价显示SIRC疫苗安全性和耐受性良好。针对新冠病毒,SIRC免疫组诱导了针对新冠病毒变异株的交叉中和抗体,CD4+T细胞免疫反应显著高于SIR免疫组;在A/California/04/2009 (H1N1)、A/Beijing/32/1992 (H3N2)、B/Brisbane/60/2008 (B/Victoria)和B/Florida/4/2006 (B/Yamagata)等四种流感病毒株的致死性攻毒实验中,SIRC疫苗组受试小鼠全部存活,防护效果优于单独的流感疫苗;在RSV攻毒实验中,SIRC免疫组小鼠肺部病毒滴度和组织病理学评分显著优于单价RSV疫苗。综上,相较于未添加佐剂的SIR疫苗,SIRC在抗体水平、细胞免疫和保护效果方面均表现更加出色,证明了CpG佐剂在联合疫苗中的关键增强作用。
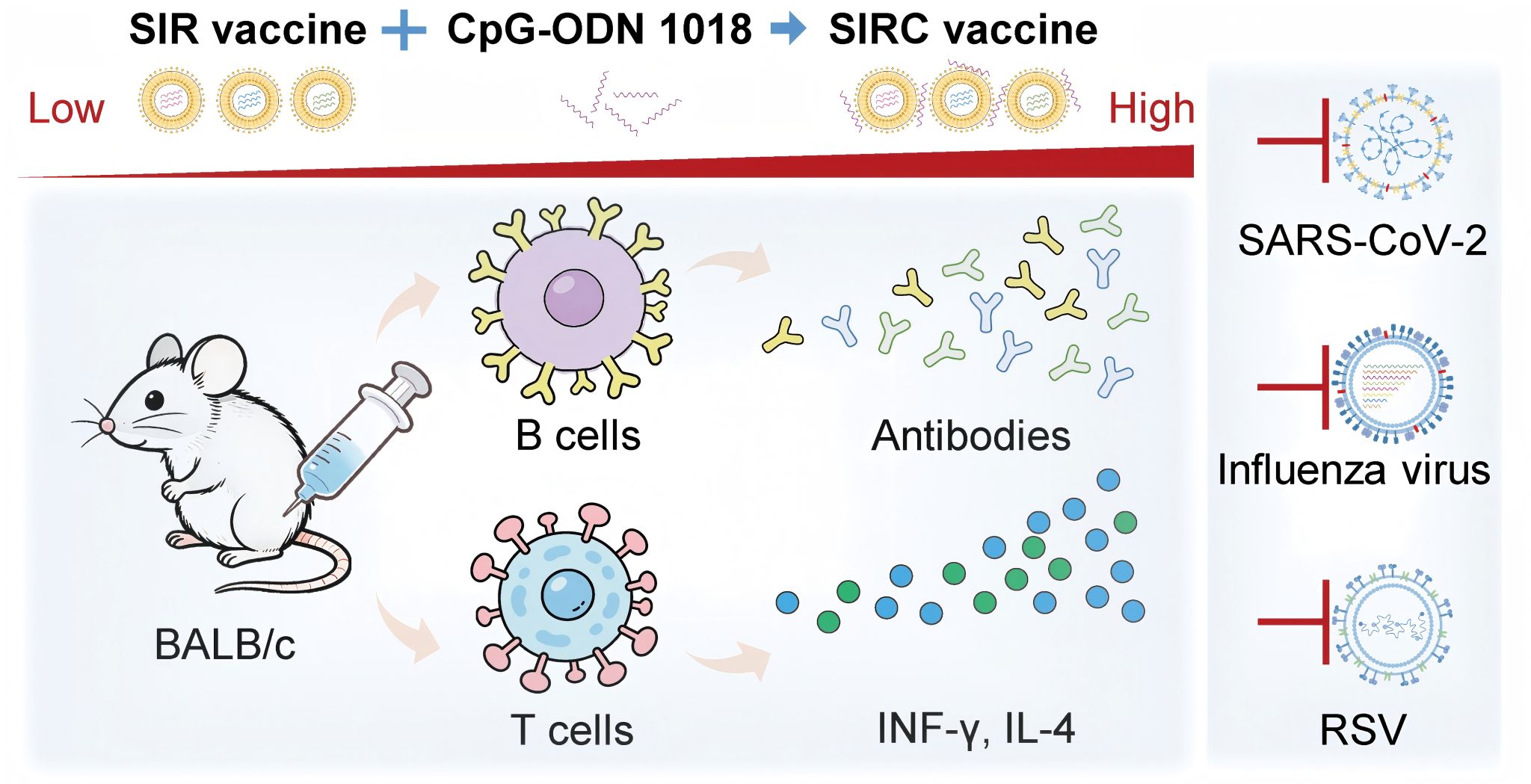
图 SIRC联合疫苗诱导针对新冠病毒、流感病毒和RSV的免疫应答
总而言之,该研究成功开发了一种同时靶向新冠病毒、流感病毒及RSV的八价mRNA联合疫苗,并验证了技术可行性,为多病原体联合mRNA疫苗设计构建了全新框架。团队通过创新的佐剂-抗原优化策略,有效破解了多抗原联合中的关键难题——抗原竞争与Th1免疫极化,实现了各抗原组分的免疫平衡与协同增强。面对呼吸道病毒叠加流行常态化的严峻挑战,SIRC疫苗为“一针三防”提供了可行的技术路径。值得一提的是,团队前期基于已上市戊肝疫苗颗粒开发了一种“即插即用”式联合疫苗平台p239:NB-RHF,同样实现了对新冠、流感、RSV和戊肝病毒的联合保护(Nat Biomed Eng 2025)。两种方案分别利用蛋白纳米颗粒平台的模块化组装优势和mRNA平台的抗原组合灵活性,展现了联合疫苗应对呼吸道病毒叠加流行的多元化技术路径。
近日,该研究成果以题为“Combination mRNA Vaccine Adjuvanted with CpG Oligodeoxynucleotides Enhances Protection against Respiratory Virus Infection”的研究论文在线发表于ACS Nano。我院崔玲艳、张思博、曾雅容、张丽敏、林敏为该论文的共同第一作者。我院李少伟教授、李婷婷、顾颖副教授和张雅丽助理教授为该论文的共同通讯作者。该研究获得国家重点研发计划、国家自然科学基金、中央高校基本科研业务费、厦门市产学研项目和翔安创新实验室的资助与支持。
论文链接:
https://pubs.acs.org/doi/10.1021/acsnano.5c14408
(公共卫生学院)