据估计,全球范围内每年新发宫颈癌病例约66万例,导致约35万例死亡。高危型人乳头瘤病毒(human papillomavirus,HPV)持续性感染是宫颈癌的主要病因,其中HPV 16/18/31/33/45/52/58型共导致了全球约95%的侵袭性宫颈癌(ICC)病例。覆盖多种型别的高价次HPV疫苗是彻底消除宫颈癌必不可缺的。全球首个九价HPV疫苗(Gardasil®9)于2014年获批上市,但其供应有限且价格高昂,在中低收入国家的可及性面临挑战。我院夏宁邵教授团队与万泰生物联合研制的九价HPV疫苗(馨可宁®9)于2025年5月在中国获批上市,成为我国首个、全球第二个上市的九价HPV疫苗。该疫苗基于独有的大肠杆菌原核表达类病毒颗粒疫苗技术体系研发,已在大规模随机对照Ⅲ期临床试验中证实对相关HPV型别持续感染出色的保护效力及安全性。
作为临床研发阶段的重要试验之一,我院研究团队于2021年开展的一项馨可宁®9与Gardasil®9的头对头研究直接比较二者的免疫应答效果。这项严格的随机对照试验证实,18~26岁中国女性全程接种后1个月(第7个月)时,馨可宁®9可诱导出非劣效于Gardasil®9的HPV型别特异性免疫应答,提示其可能具有与Gardasil®9相似的保护效力(Lancet Infect. Dis. 2023)。
现有研究证据表明,HPV疫苗接种后约1个月,抗体水平达到峰值,随后迅速下降,在接种后2-3年进入平台期,并在随后数年内保持相对平稳。评估HPV疫苗免疫反应平台期抗体水平对揭示疫苗的长期保护潜力具有重要意义。因此,为了比较馨可宁®9和Gardasil®9的平台期抗体水平,研究团队邀请头对头研究中的487名志愿者继续参加第3年的随访观察,最终403人(馨可宁®9组200人,Gardasil®9组203人)完成血样采集。在免疫持久性的符合方案集(PPS-P)中,馨可宁®9组HPV 6/16/31/33/45/52/58型的中和抗体几何平均浓度(GMC)略高于Gardasil®9组,而HPV 11/18型的GMC略低于Gardasil®9组,九种型别的GMC比值(馨可宁®9/Gardasil®9)范围为0.78~1.91。值得关注的是,所有型别GMC比值的95%置信区间下限值均高于预设的非劣效标准。此外,两组的血清抗体阳性率均维持在较高的水平:馨可宁®9组为84.7%~100.0%,Gardasil®9组为86.2%~100.0%。在三年内,两组各型别的抗体衰减趋势一致。
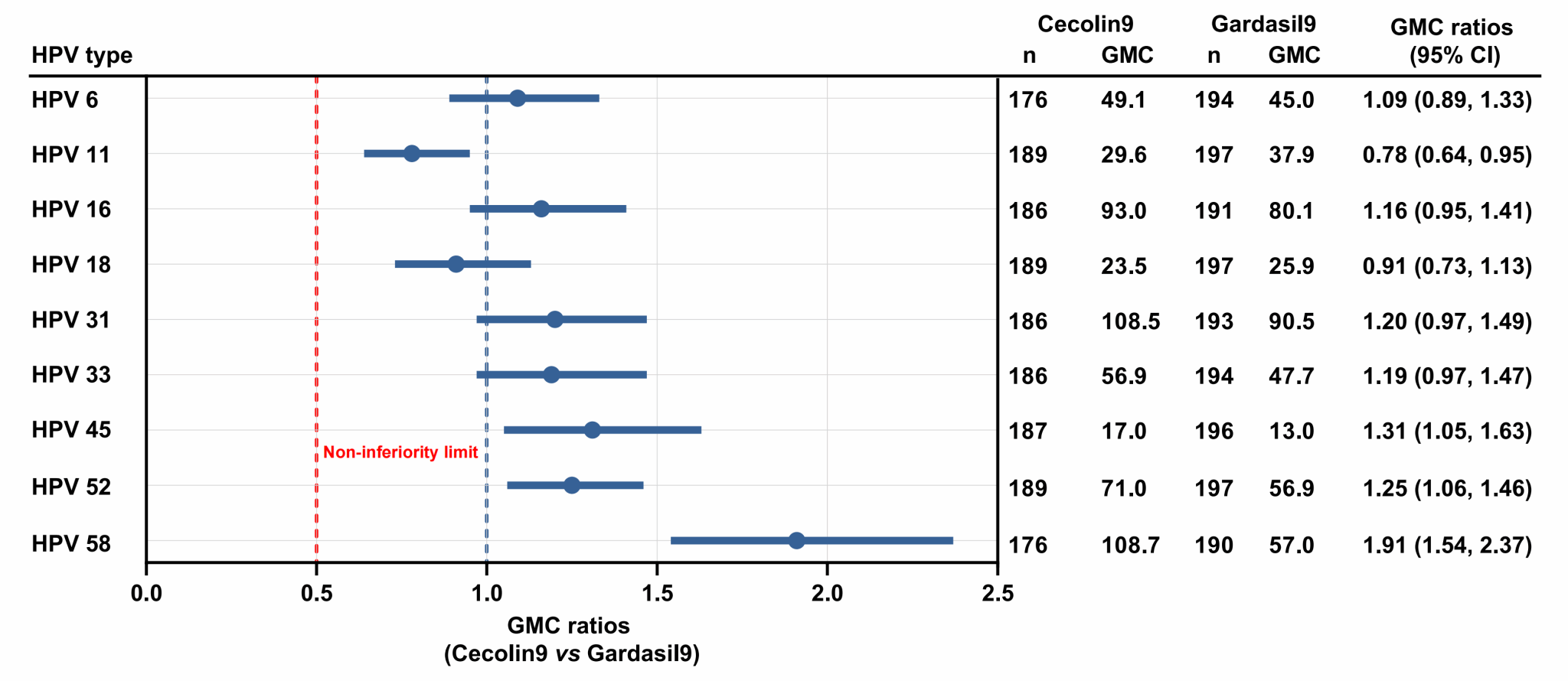
图 馨可宁®9和Gardasil®9在抗体平台期的中和抗体GMC比值
这项拓展研究证明了馨可宁®9诱导产生的HPV型别特异性抗体在免疫反应平台期的抗体水平与Gardasil®9相当,提示其具有与Gardasil®9相似的长期免疫保护潜力。随着研究证据的不断累积,馨可宁®9对相关HPV型别的持久保护效力得到进一步证实,为其今后的临床应用提供了更完整、更坚实的循证依据。
近日,该研究成果以题为“Immunogenicity comparison of an Escherichia coli-produced 9-valent human papillomavirus vaccine and Gardasil9 in Chinese women aged 18-26 years: three-year follow-up data from a randomised clinical trial”的论文在线发表于《柳叶刀-区域健康(西太平洋)》(The Lancet Regional Health-Western Pacific)。我院博士研究生钟国华、博士后毕兆峰,江苏省疾病预防控制中心储凯,中国食品药品检定研究院张黎为该论文共同第一作者。我院张军教授,吴婷教授,江苏省疾病预防控制中心潘红星,中国食品药品检定研究院黄维金为该论文的共同通讯作者。该研究获得了国家重点研发计划、国家自然科学基金、北京市自然科学基金、中央高校基本科研业务费专项基金资助、厦门大学研究生田野调查基金和厦门万泰沧海生物技术有限公司的支持。
论文链接:https://www.thelancet.com/journals/lanwpc/article/PIIS2666-6065(25)00210-X/fulltext
(公共卫生学院)